Märkning av kosttillskott
Reglerna om hur ett kosttillskott ska märkas gäller utöver de allmänna märkningsreglerna, som berör alla livsmedel. Här hittar du märkningsreglerna för kosttillskott.
- Obligatorisk livsmedelsinformation för kosttillskott
- Specifika märkningskrav för kosttillskott
- Hyllkantsmärkning
- Alkoholhaltiga kosttillskott
- Frivillig information
- Näringspåståenden om kosttillskott
- Hälsopåståenden om kosttillskott
- ”Naturlig”
- ”Bör inte ätas av…”
- Påståenden om förbättrat utseende
Obligatorisk livsmedelsinformation för kosttillskott
Generella märkningskrav
Kosttillskott säljs färdigförpackade och ska märkas enligt kraven i förordning (EU) nr 1169/2011. De obligatoriska uppgifterna omfattar bland annat ingrediensförteckning, beteckning, datummärkning, kontaktuppgifter, allergimärkning och nettokvantitet.
För livsmedel vars karaktär och egenskaper påverkas av ingrediensernas beredningsform, det vill säga hur ingredienserna är behandlade, ska beredningsformen framgå av märkningen. Uppgifter om livsmedlets fysiska tillstånd eller särskilda behandling ska finnas i anslutning till beteckningen, till exempel pulverisering, koncentrering eller liknande. Sådana uppgifter kan behövas för att inte vilseleda eller för att inte innebära en hälsorisk för konsumenten. Se artikel 17.5 och bilaga VI till förordning (EU) nr 1169/2011.
Obligatorisk information - färdigförpackade livsmedel
Nedan visas ett exempel på en kosttillskottsetikett med obligatorisk märkning för en multivitamin med vitaminer och mineralämnen. Särskilda villkor för förvaring, bruksanvisning och allergimärkning har utelämnats för ökad tydlighet. Siffrorna i bilden är en hänvisning till beskrivningarna under bilden.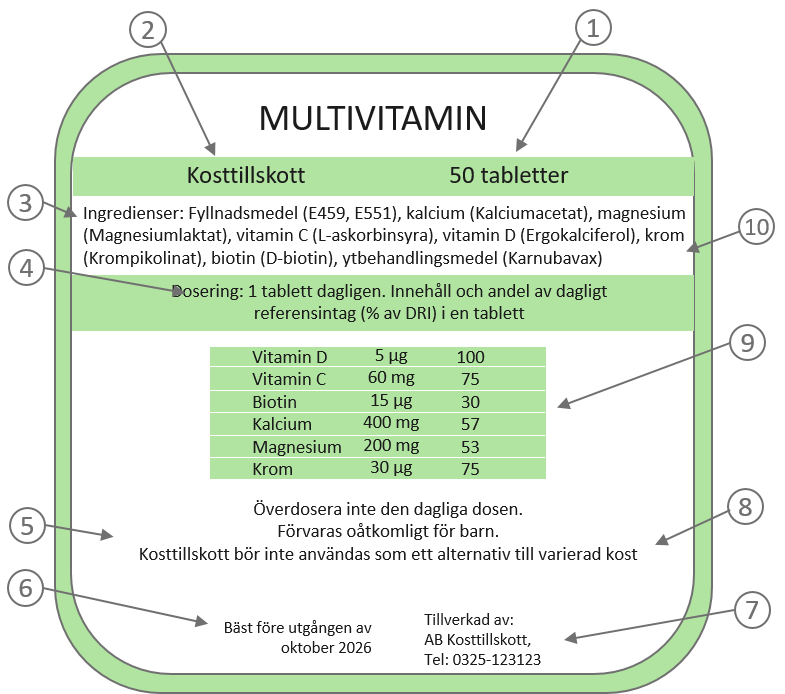
- Nettokvantiteten på förpackningar med tabletter, kapslar eller liknande får lämnas genom att ange uppgiften om antalet tabletter, kapslar eller liknande enligt 7 § LIVSFS 2014:4.
- Den beteckning som ska användas på alla kosttillskott är ”kosttillskott”. Kosttillskott är en föreskriven beteckning, se 4 § LIVSFS 2023:3 och artikel 17 i förordning (EU) nr 1169/2011.
- Ingrediensförteckning måste anges på färdigförpackade livsmedel, se artikel 9.1 b, 17 och 18 i förordning (EU) nr 1169/2011. I ingrediensförteckningen anges vitaminets eller mineralets vedertagna beteckning. Det är frivilligt att även ange vitamin- och mineralföreningen. I bilaga II till den konsoliderade versionen av direktiv 2002/46/EG finns alla vitamin- och mineralföreningar som får ingå i kosttillskott listade.
- En rekommenderad daglig dos av kosttillskottet ska anges enligt 6 § 2 p LIVSFS 2023:3. Den rekommenderade dagliga dosen kan till exempel vara 1 tablett dagligen.
- Specifika märkningskrav för kosttillskott anges i 6 § och 8 § LIVSFS 2023:3. Dessa omfattar namn eller beskaffenhet på de ämnen som kännetecknar produkten, en rekommenderad daglig dos, en varning om att inte överskrida den dagliga dosen, att kosttillskott inte bör användas som ett alternativ för en varierad kost, uppgiften om att förvara produkten utom räckhåll för små barn samt mängd av de näringsämnen och andra ämnen som ingår i produkten.
- Artikel 9.1 f i förordning (EU) nr 1169/2011 ställer krav på att bäst före eller sista förbrukningsdag anges.
- Enligt artikel 9 h och 8.1 i förordning (EU) nr 1169/2011 ska kontaktuppgifter anges till företaget som är ansvarig för livsmedelsinformationen.
- Artikel 15 i förordning (EU) nr 1169/2011 anger språkkrav. I 5 § LIVSFS 2014:4 anges att uppgifterna ska vara på svenska.
- Mängden näringsämnen i den rekommenderade dagliga dosen ska anges. Vitaminer och mineraler anges i procent av de referensvärden som anges i bilaga XIII till Europaparlamentets och rådets förordning (EU) nr 1169/2011, se 9 § LIVSFS 2023:3.
- I ingrediensförteckningen ska tillsatser anges med ett kategorinamn följt av livsmedelstillsatsens specifika beteckning (namn) och/eller E-nummer. Artikel 18 och bilaga VII till förordning (EU) nr 1169/2011 anger hur tillsatser ska anges i ingrediensförteckningen. Förordning (EG) nr 1333/2008 reglerar tillsatser.
Ingrediensförteckning
I kosttillskott ingår ofta växter eller växtbaserade extrakt, så kallade botanicals. Livsmedelsverket anser att det svenska artnamnet på alla ingående växter, till exempel ”maskros” och ”svartpeppar”, ska användas i ingrediensförteckningen. Om svenskt namn saknas bör det latinska namnet med både släktnamn och artnamn användas. Vid kontroll ska tillverkare kunna verifiera märkningen, det vill säga bland annat visa dokumentation som styrker ingrediensförteckningen. Till exempel genom att visa att samma växt, djur eller organism som ingår i produkten anges i märkningen. Om ingrediensförteckningen översätts från ett annat språk kan namnet på en växt blandas ihop med någon annan växt med liknande namn.
På kosttillskott som baseras på djur eller andra organismer, till exempel extrakt från djurorgan, alger eller svampar, bör samma krav ställas som på kosttillskott baserade på växter.
Extraktions- och lösningsmedel som har använts ska inte anges i märkningen, men ska kunna anges vid kontroll hos tillverkaren. Om medlen finns kvar i den färdiga produkten ska de anges i ingrediensförteckningen. Olika extraktions- och lösningsmedel löser ut olika mycket av olika verksamma ämnen. Vanligtvis används etanol som lösningsmedel.
Ett mycket vanligt märkningsfenomen, framför allt på kosttillskott från USA, är så kallade ”proprietary blends” eller andra ”blends”, blandningar av ingredienser under ett visst varumärke. I märkningen anges mängden av ämnena i sin helhet, utan att de enskilda ingredienserna i blandningen deklareras mängdmässigt enligt LIVSFS 2023:3. Sådan märkning är således inte tillåten. Att det inte framgår hur mycket av de verksamma ämnena som finns i ett kosttillskott kan innebära hälsorisker.
Flera av de vitamin- och mineralföreningar som får ingå i kosttillskott som näringsämnen kan även användas som livsmedelstillsatser. För dem finns renhetskrav fastställda i reglerna om tillsatser. Kraven gäller också för vitaminer och mineraler som ingår som näringsämnen i kosttillskott. Se 11 § LIVSFS 2023:3. Kosttillskott finns med som en egen livsmedelskategori i bilaga II till förordning (EG) nr 1333/2008. Huvudsyftet med användningen av ett ämne avgör hur det ska anges i ingrediensförteckningen.
Vitaminer och mineraler ska anges i ingrediensförteckningen på samma sätt som när de ingår i andra livsmedel. För nya livsmedel är det benämningen i unionsförteckningen som ska användas i märkningen.
Vitamin- och mineralkällor
Kontroll av tillsatser
Beteckningar för ingredienser
Exempel på vitaminer som kan ingå i kosttillskott som tillsats eller vitamin
- Askorbinsyra (vitamin C) som antioxidationsmedel
- Riboflavin (vitamin B2) som färgämne
Ytterligare obligatoriska uppgifter
För vissa typer eller kategorier av livsmedel krävs ytterligare obligatoriska uppgifter, utöver de uppgifter som nämns i artikel 9.1. i förordning (EU) nr 1169/2011. Se punkt 4.2 i bilaga III artikel 10.1 och bilaga III till samma förordning.
Exempel på livsmedel med krav på ytterligare obligatorisk märkning
- Livsmedel som förpackats i en skyddande atmosfär
- Livsmedel som innehåller sötningsmedel
- Livsmedel som innehåller glycyrrhizinsyra
- Livsmedel som innehåller växtsteroler
- Livsmedel som innehåller koffein
Specifika märkningskrav för kosttillskott
Utöver märkningskraven i förordning (EU) nr 1169/2011, ska kosttillskott även vara märkta med de obligatoriska uppgifterna som anges i § 4, 6 och 8 i LIVSFS 2023:3.
- Beteckningen kosttillskott
- Uppgift om att produkterna bör förvaras utom räckhåll för små barn
- Namnet på de kategorier av näringsämnen eller ämnen som kännetecknar produkten, eller en uppgift om beskaffenheten av dessa näringsämnen eller ämnen
- Uppgift om att kosttillskott inte bör användas som ett alternativ till en varierad kost
- Mängd av näringsämnen eller andra ämnen med näringsmässig eller fysiologisk verkan
- Rekommenderad daglig dos
- En varning för att överskrida den angivna rekommenderade dagliga dosen
Beteckning
Livsmedel som uppfyller kraven enligt föreskrifterna ska märkas med beteckningen kosttillskott. Huvudsyftet med märkningsreglerna är att konsumenten inte ska vilseledas. Beteckningen ska därför framgå tydligt, oavsett hur den presenteras i märkningen.
Det finns inga krav om var i märkningen beteckningen ska finnas, utom att den ska anges på väl synlig plats och i samma synfält som uppgifter om nettokvantitet och eventuell alkoholhalt. Se LIVSFS 2023:3 och artikel 13.1 och 13.5 i förordning (EG) nr 1169/2011.
I vissa fall har det betydelse om en produkt säljs under beteckningen kosttillskott eller inte. Vissa ämnen regleras av förordning (EU) nr 2015/2283 om de används i andra produkter än kosttillskott. Dessutom kan vissa tillsatser vara förbjudna att använda i andra produkter än kosttillskott.
Förvaras utom räckhåll för små barn
På kosttillskott ska det framgå att produkten ska förvaras utom räckhåll för små barn. För höga doser av vitaminer och mineralämnen kan vara skadliga för hälsan. Järntabletter kan exempelvis vara giftiga för barn även i relativt låga doser.
Kategorinamn
Kategorinamn eller uppgift om beskaffenheten ska anges på de näringsämnen eller andra ämnen som kännetecknar produkten. Med kategori menas till exempel vitaminer, fettsyror eller växtextrakt. Med beskaffenhet menas till exempel vitamin C, omega-3-fettsyror eller åkerfräkenextrakt.
Kosttillskott bör inte användas som ett alternativ till varierad kost
På förpackningen ska det stå att kosttillskott inte är ett alternativ till en varierad kost. De allra flesta får i sig tillräckligt med vitaminer och mineraler genom den vanliga maten, då finns det alltså inget behov av extra kosttillskott. Det är därför inte tillåtet att påstå eller antyda att en allsidig och varierad kost inte i allmänhet kan ge tillräckliga mängder vitaminer eller mineraler, se 7 § i LIVSFS 2023:3.
Mängd av ämnen istället för näringsdeklaration
Kosttillskott är undantagna kravet om näringsdeklaration, se artikel 29 i förordning (EU) nr 1169/2011. Det gäller oavsett om det finns ett närings- eller ett hälsopåstående. Däremot ska mängderna av de näringsämnen och ämnen med näringsmässig eller fysiologisk verkan anges med siffror och avse den mängd som ingår i den dagliga dos som tillverkaren rekommenderar. Det gäller oavsett om det verksamma ämnet är ett extrakt, bakteriekultur, kommer från en växt eller fisk etcetera. Se 2 § LIVSFS 2023:3. För bakterier eller jästsvampar deklareras mängden som antalet kolonibildande enheter (colony forming units), CFU. Det är inte möjligt att ange mängderna i procent av dagligt referensintag för andra ämnen än vitaminer och mineraler.
När det gäller växter känner man många gånger inte till den aktiva substansen. I Norden tillämpar man inte kravet att ange den aktiva substansen för växter där den uppgiften saknas. Då räcker det med att mängden av respektive art anges. På liknande sätt kan man resonera om kosttillskott med innehåll av bakteriekulturer eller enzymer.
I dagsläget finns inget godkänt hälsopåstående för bakteriekulturer eftersom den näringsmässiga eller fysiologiska verkan inte har kunnat bevisas. Det innebära att mängden ska anges men att det inte är nödvändigt att specificera stamnamnet.
I kosttillskott med fiskoljor är inte fiskarten, som den verksamma substansen utvinns ifrån, av betydelse. De verksamma substanserna i fiskolja är Omega-3-fettsyrorna DHA och EPA. Innehållet av dessa ämnen ska framgå i märkningen. Se artikel 18.4 och bilaga VII, del B punkt 5 i förordning (EU) nr 1169/2011.
Om vitaminer och mineraler ingår i produkten ska mängden av respektive vitamin och mineral anges och, i förekommande fall, i procent av dagligt referensintag (DRI), se del A.1 i bilaga XIII till förordning (EU) nr 1169/2011.
Mängderna redovisas med de namn som står i bilaga 1 till EG-direktiv 2002/46. Mängd av näringsämnen gäller den totala mängden, det vill säga både tillsatta och naturligt förekommande vitaminer och mineraler. Mängderna ska anges som genomsnittsvärden och kunna styrkas med analysprotokoll, se 8 § LIVSFS 2023:3. Om betakaroten används som A-vitaminkälla kan omräkningsfaktorn som anges i Nordiska näringsrekommendationer 2023 (NNR) användas.
DRI är baserat på europeiska data och ska inte förväxlas med de nordiska näringsrekommendationerna (NNR), som i första hand används vid kostplanering. Det finns inga speciella referensvärden för barn.
Nordiska näringsrekommendationer
Rekommenderad daglig dos
Den rekommenderade dosen ska anges som en daglig dos, det är inte tillåtet att ange en dos för till exempel varannan dag. Dosintervall ska anges med lägsta och högsta dos, till exempel 2-3 tabletter 1-2 gånger dagligen. Se 8 § LIVSFS 2023:3. Det ska alltså stå på förpackningen hur mycket lägsta och högsta rekommenderad dos innehåller.
Varning för att överskrida den dagliga dosen
I 6 § 3 p LIVSFS 2023:3 framgår det att kosttillskott ska märkas med en varning för att överskrida den angivna rekommenderade dagliga dosen. Denna uppgift ska finnas med oavsett om det finns hälsorisker med att överskrida den dagliga dosen eller inte.
Hyllkantsmärkning
Hyllkants- och hyllsektionsmärkning kan ibland innehålla både närings- och hälsopåståenden. Presentationen av ett livsmedel får inte vara vilseledande. Hyllkantsmärkningen måste därför stämma överens med märkningen på förpackningen. Produkternas placering är också viktig i förhållande till hänvisningen av produktkategori i skyltmaterial med mera. Kosttillskott bör aldrig vara placerade så att de av konsumenterna kan uppfattas som läkemedel och vice versa.
Alkoholhaltiga kosttillskott
Kosttillskott och tinkturer som innehåller mer än 2,25 volymprocent alkohol och ska säljas till konsument får innehålla högst 30 gram etanol per förpackning.
Produkten ska innehålla komponenter som så starkt påverkar lukt, smak och färg att det så långt som möjligt hindrar annan användning av preparatet än som kosttillskott. Om kosttillskott påträffas som inte uppfyller dessa krav bör Folkhälsomyndigheten kontaktas. Se 11 § och 4.3 p tabell 4 Folkhälsomyndighetens föreskrifter och allmänna råd (HSLF-FS 2022:63) om teknisk sprit och alkoholhaltiga preparat.
Det är inte tillåtet att göra hälsopåståenden för alkoholhaltiga drycker på mer än 1,2 % vol. alkohol, se artikel 4.3 i förordning (EU) nr 1169/2011. Kosttillskott i flytande form är inte en alkoholhaltig dryck vilket innebär att det är möjligt att göra hälsopåståenden på alkoholhaltiga kosttillskott.
Frivillig information
Utöver de uppgifter som är föreskrivna för livsmedel generellt genom förordning (EU) nr 1169/2011 och för kosttillskott genom LIVSFS 2023:3 kan företagare ge annan, frivillig information i märkningen. Den frivilliga märkningen ska kontrolleras med stöd i förordning (EU) nr 1169/2011 eller i annan lagstiftning som syftar till att ge konsumenten relevant och korrekt information om produktens egenskaper och förväntade effekter, till exempel när det gäller närings- och hälsopåståenden.
Näringspåståenden om kosttillskott
Näringspåståenden är påståenden om att ett livsmedel har ett visst hälsosamt näringsinnehåll. De näringspåståenden som får användas är listade i bilagan till förordning (EG) nr 1924/2006. Det är även möjligt att använda Livsmedelsverkets kostråd i märkning och marknadsföring under vissa förutsättningar.
Närings- och hälsopåståenden
Näringspåståenden
Livsmedelsverkets kostråd
Reglerna om näringspåståenden gäller alla frivilliga märkningsuppgifter på livsmedel (inklusive kosttillskott). Obligatoriska märkningsuppgifter omfattas inte av reglerna för näringspåståenden, se artikel 1.2 och 2.2.1 i förordning (EG) nr 1924/2006. Det är därmed tillåtet att på kosttillskott på ett neutralt sätt ange namnet kategorier eller beskaffenhet av näringsämnen eller ämnen som kännetecknar produkten utan att den uppgiften omfattas av reglerna för näringspåståenden.
Exempel på obligatorisk märkning som inte är näringspåståenden
Ett kosttillskott har namnet ”Multivitamin”. Namnet informerar konsumenten om att de ämnen som är karaktäristiska för produkten tillhör kategorin vitaminer.
I märkningen på ett kosttillskott anges ”mjölksyrabakterier”. Informationen motsvarar kravet på att ange kategorin på de ämnen som kännetecknar produkten.
En brustablett har namnet ”C-vitaminbrus”. Namnet informerar konsumenten om beskaffenheten hos det ämne som kännetecknar kosttillskottet.
Kategorier av näringsämnen eller ämnen som kännetecknar produkten, eller en uppgift om beskaffenheten av dessa näringsämnen eller ämnen ska anges på kosttillskott enligt 6 § 1 p LIVSFS 2023:3.
I vissa fall kan uppgiften om ett innehåll vara ett hälsopåstående till exempel ”innehåller antioxidanter” eller ”innehåller probiotika”.
Högt innehåll
Information om högt innehåll av ett näringsämne eller annat ämne i ett kosttillskott går utöver de krav som är obligatoriska i regelverket om kosttillskott. Den typen av information regleras därför av förordning (EG) nr 1924/2006 om närings- och hälsopåståenden. En alternativ formulering till högt innehåll är ”rik på”.
Näringspåståenden om innehåll och högt innehåll
Lågt eller minskat innehåll
Information om lågt eller minskat innehåll av ett näringsämne eller annat ämne i ett kosttillskott är frivillig information som regleras av förordning (EG) nr 1924/2006 om närings- och hälsopåståenden eftersom det inte finns sådana krav på information i LIVSFS 2023:3. Sådana påståenden får endast göras om näringsämnen eller ämnen där det är dokumenterat gynnsamt med ett lågt innehåll. Eftersom kosttillskott per definition ska vara en koncentrerad källa till näringsämnen eller andra ämnen med näringsmässig eller fysiologisk verkan så är den här typen av påståenden ofta inte möjliga att göra på kosttillskott.
Näringspåståenden om lågt innehåll
Mängdvillkor
För näringspåståenden anges mängdvillkoren för respektive påstående i bilagan till förordning (EG) nr 1924/2006. Villkoren uttrycks på olika sätt för de olika påståendena, i de flesta fall med mängd per 100 gram, 100 ml eller 100 kcal. Villkoren för påståenden om att ett livsmedel utgör en källa till respektive har ett högt innehåll av ett vitamin och/eller mineralämne anges dock inte numeriskt. För sådana påståenden gäller att produkten måste innehålla minst en betydande mängd enligt bilaga XIII till förordning (EU) nr 1169/2011, respektive dubbla den mängden, av vitaminet eller mineralämnet.
Villkoren är enligt Livsmedelsverkets bedömning inte fullt ut anpassade efter kosttillskott, vilka konsumeras i små mängder. Av de allmänna villkoren för användning av näringspåståenden följer att den mängd av en produkt som rimligtvis kommer att konsumeras ska innehålla betydande mängd av det näringsämne eller annat ämne som påståendet gäller (se artikel 5.1 d i förordning (EG) nr 1924/2006). Livsmedelsverket anser därför att mängdvillkoren enligt bilagan till förordning (EG) nr 1924/2006 bör sättas i relation till den rekommenderade dagliga dosen, vad gäller kosttillskott. En bedömning måste dock göras i det enskilda fallet.
Observera att det är obligatoriskt att i märkningen av kosttillskott ange mängderna av de näringsämnen och ämnen med näringsmässig eller fysiologisk verkan som ingår i produkterna i numerisk form, enligt 8 § LIVSFS 2023:3, vilket motsvarar det godkända påståendet ”källa”. Den obligatoriska uppgiften ska inte betraktas som ett näringspåstående.
Näringspåståendet om högt innehåll om ett kosttillskott
För att det ska vara relevant att göra ett näringspåstående om högt innehåll av järn i ett kosttillskott bör den dagliga dosen av kosttillskottet innehålla minst 30 % av det dagliga referensintaget (DRI) för järn, det vill säga dubbelt så mycket som den betydande mängden.
Näringspåståenden om innehåll och högt innehåll
Näringsdeklaration är inte obligatoriskt på kosttillskott
I reglerna för närings- och hälsopåståenden anges att näringsdeklaration är obligatorisk när sådana påståenden görs. Men det märkningskravet är bara relevant för andra kategorier av livsmedel än kosttillskott, se artikel 7 i förordning (EG) nr 1924/2006. Näringsvärdena i kosttillskott ska anges enligt reglerna i LIVSFS 2023:3. Därmed behöver inte innehållet av bland annat energi, protein eller fett anges på kosttillskott. Skälet är att innehållet av dessa energibärande komponenter ofta är försumbart och är därmed inte relevant att ange.
Specifika märkningskrav för kosttillskott - mängd av ämnen istället för näringsdeklaration
Hälsopåståenden om kosttillskott
Hälsopåståenden är alla typer av påståenden om livsmedel som uttrycker att det har hälsofördelar för konsumenten.
Närings- och hälsopåståenden
Hälsopåståenden
Endast godkända hälsopåståenden eller allmänna hälsopåståenden som åtföljs av ett relevant godkänt hälsopåstående får göras. På EU-kommissionens webbplats finns en databas som innehåller samtliga påståenden som har, eller inte har, blivit godkända. Det är till viss del möjligt att omformulera det godkända hälsopåståendet så länge innebörden av påståendet är den samma. Endast de hälsopåståenden som är godkända enligt artikel 14.1b i förordning (EG) nr 1924/2006 får användas på kosttillskott till barn.
Nedan visas ett exempel på en etikett på ett kosttillskott med ett godkänt hälsopåstående. I exemplet är viss obligatorisk information utelämnad för ökad tydlighet. Siffrorna i bilden är en hänvisning till beskrivningarna under bilden.
- Hälsofrämjaren är ett exempel på ett varumärke som är ett hälsopåstående. Därmed krävs att det åtföljs av ett godkänt närings- eller hälsopåstående enligt artikel 10.3 i förordning (EG) nr 1924/2006.
- Hälsopåståendet ”bidrar till normal muskelfunktion” är godkänt för både kalcium och magnesium. Eftersom det är tillåtet att göra en viss förändring av ordalydelsen i ett godkänt hälsopåstående är det tillåtet att kombinera mineralämnena i samma påstående under förutsättning att villkoren för de båda hälsopåståendena uppfylls.
- Uttrycket ”Kosttillskott bör inte användas som ett alternativ till varierad kost. Det är också viktigt med en hälsosam livsstil” är ett förslag på hur det är möjligt att kombinera obligatoriska märkningsuppgifter för kosttillskott och livsmedel med närings- och hälsopåståenden enligt 6 § 4 p LIVSFS 2023:3 och artikel 10.2 i förordning (EG) nr 1924/2006.
EU-kommissionens register över närings- och hälsopåståenden
Allmänna hälsopåståenden
Formulering av godkända hälsopåståenden
Påståenden om barns utveckling och hälsa
Innan ett hälsopåstående godkänns så utvärderas den vetenskapliga bevisningen av Europeiska myndigheten för livsmedelssäkerhet (Efsa). Om en hälsoeffekt kan visas med det underlag som har lagts fram så kan hälsopåståendet bli godkänt av EU-kommissionen. Eftersom alla hälsopåståenden är ”vetenskapligt bevisade”, har en ”dokumenterad effekt” och är ”noga undersökta” så anser Livsmedelsverket att sådana uttryck är vilseledande, artikel 3 a i förordning (EU) nr 1924/2006.
Nedan visas ett exempel på en etikett på ett kosttillskott med icke godkända hälsopåståenden. I exemplet är viss obligatorisk information utelämnad för ökad tydlighet. Siffrorna i bilden är en hänvisning till beskrivningarna under bilden.
- Fantasinamnet Energibooster är ett allmänt ospecifikt hälsopåstående. Allmänna hälsopåståenden måste enligt artikel 10.3 i förordning (EG) nr 1924/2006 åtföljas av ett godkänt hälsopåstående. Fantasinamnet åtföljs i exemplet av ett icke godkänt hälsopåstående om att koffein skulle öka den fysiska prestationen under kortvarig högintensiv träning. Därmed är fantasinamnet inte tillåtet.
- Det är inte tillåtet att antyda eller ange att näringsinnehållet i vanlig mat inte ger tillräckliga mängder av näringsämnen, till exempel genom att säga att vitaminhalten i mat har sjunkit så att risken för att få brist på vitaminet ökat. Det är inte heller tillåtet att skapa otrygghet eller rädsla för förändringar i fysiologiska funktioner, enligt artikel 3 d och e i förordning (EG) nr 1924/2006 samt 7 § LIVSFS 2023:3.
- Hälsopåståenden beskriver vad ett visst ämne, ett livsmedel eller en livsmedelskategori har för effekt. Påståenden om att hälsoeffekten kommer från produkten i sig är därför inte tillåtna enligt artikel 10.3 och 13 i förordning (EG) nr 1924/2006. Påståendet ”Energibooster bidrar till att minska trötthet och utmattning” är ett exempel på en sådan otillåten formulering.
- Hälsopåståenden om koffein och ökad fysisk prestationsförmåga under kortvarig högintensiv träning har utvärderats och är inte godkänt. Det är alltså inte tillåtet att använda.
- Alla godkända hälsopåståenden har blivit utvärderade innan de godkändes, det innebär att de har vetenskapligt stöd. Det är därför vilseledande att ange att hälsopåståenden har vetenskapligt stöd eftersom konsumenten då kan tro att bara vissa har det, se artikel 3 a i förordning (EG) nr 1924/2006.
- Påståenden som hänvisar till rekommendationer av enskilda fackmän inom hälsoområdet är inte tillåtna, se artikel 11 och 12 i förordning (EG) nr 1924/2006. Det är alltså inte möjligt att skriva att produkten rekommenderas av dietisten Anna Andersson.
- Det är endast tillåtet att ange dagligt referensintag eller dagsbehov för vitaminer och mineraler. För andra ämnen, till exempel koffein eller flavanoider finns inget särskilt dagsbehov fastställt. Därför är det inte möjligt att i märkningen skriva att ”dagsbehovet av koffein är säkrat”.
Märkningskrav om varierad kost
När ett hälsopåstående görs ska uppgiften vikten av en mångsidig och balanserad kost och en hälsosam livsstil anges i märkningen, se artikel 10 i förordning (EG) nr 1924/2006. För kosttillskott finns kravet att ange att kosttillskott inte bör användas som ett alternativ till en varierad kost, se 6 § 4 p LIVSFS 2023:3. Eftersom inget av märkningskraven är ordagrant styrda så finns det ingen anledning att ange dessa uppgifter på två ställen.
Obligatoriska tilläggsuppgifter till hälsopåståenden
Hälsopåståenden på alkoholhaltiga kosttillskott
Det är inte tillåtet att göra hälsopåståenden för alkoholhaltiga drycker på mer än 1,2 % vol. alkohol, se artikel 4.3 i förordning (EU) nr 1169/2011. Kosttillskott i flytande form är inte en alkoholhaltig dryck, vilket innebär att det är möjligt att göra hälsopåståenden på alkoholhaltiga kosttillskott.
Botanicals
Botanicals (växter) är det engelska samlingsnamnet för en grupp av ämnen som inbegriper hela växter, delar av växter och växtextrakt. Botanicals används ofta i kosttillskott.
Ett stort antal hälsopåståenden om botanicals har ännu inte blivit utvärderade av Europeiska myndigheten för livsmedelssäkerhet (Efsa) vilket innebär att inget beslut har tagits av EU-kommissionen om de är godkända eller inte. Tills beslut tagits är det tillåtet att göra de hälsopåståenden man ansökt om, under eget ansvar.
Företagarna ska vid kontroll kunna visa att de hälsopåståenden om botanicals som de gör i märkningen tillhör de påståenden som inlämnades till Efsa för utvärdering före den 31 januari 2008. Vid förfrågan ska de också kunna hänvisa till vetenskapligt stöd för hälsopåståendet, den rekommenderade dosen samt att beredningsmetoden av botanicals motsvarar den som beskrivs i anmälan av hälsopåståendet.
”Naturlig”
Begreppet bör användas med försiktighet i märkningen av kosttillskott. Kosttillskott utgörs till stor del av processade råvaror och överensstämmer därmed inte Livsmedelsverkets tolkning av begreppet ”naturlig”. För att inte riskera att vilseleda konsumenten om kosttillskottets natur kan det vara tydligare att i relevanta fall ange att kosttillskottet eller substanser i kosttillskottet framställs ur en naturlig råvara.
Naturlig, naturprodukt, natur-
”Bör inte ätas av…”
Kosttillskott, liksom alla andra livsmedel, ska ha en sammansättning som inte medför hälsorisker. Kosttillskottens sammansättning och eventuella innehåll av allergener måste därför anges i märkningen. Innehåll av vissa ingredienser medför krav att i märkningen ange att livsmedlet har hög halt av ingrediensen eller att vissa konsumentgrupper bör undvika livsmedlet. Se punkt 4.2 i bilaga III till förordning (EU) nr 1169/2011, artikel 10.1 och bilaga III till samma förordning.
Andra varningar bör bedömas från fall till fall. Varningar, till exempel om att produkter inte bör konsumeras av personer med hjärtsjukdom, diabetes eller ledbesvär, gravida, barn eller ammande kan ha ett berättigande om företagaren kan ange skälen för denna varning.
Påståenden om förbättrat utseende
Påståenden om att substanser eller produkter kan resultera i ökad lyster i håret, förbättrad andedräkt, färre rynkor etcetera är inte hälsopåståenden enligt definitionen i förordning (EG) nr 1924/2006. De omfattas därmed inte heller av villkoren i denna förordning. Det finns inga specifika rättsakter som reglerar skönhetspåståenden, ”beauty claims”, utan de omfattas av de generella märkningsreglerna.
Om skönhetspåståenden görs i märkning eller annan marknadsföring ska företagaren kunna uppvisa vetenskapligt stöd för dessa, i annat fall är de att beteckna som vilseledande. Gränsdragningen mellan hälsopåståenden och skönhetspåståenden måste avgöras från fall till fall. Se artikel 7 i förordning (EU) 1169/2011.
En europeisk sammanslutning av kosttillskottsföretag, Food Supplements Europe, har utarbetat riktlinjer för gränsdragning mellan hälsopåståenden och skönhetspåståenden samt för hur vetenskapliga studier bör vara uppbyggda i syfte att utveckla substanser och produkter för ökad skönhet.
Food Supplements Europe - our publications and guidelines